COCCIDIOSIS INTESTINALES Y TISULARES (Sarcocistosis)
Podcast
Videos
Resumen
La sarcocistosis, una infección zoonótica causada por el parásito protozoario Sarcocystis, afecta tanto a animales como a humanos, presentando dos formas principales: intestinal y muscular. La transmisión intestinal ocurre por el consumo de carne cruda o mal cocida, mientras que la muscular se da por la ingesta de esporoquistes en alimentos contaminados. Aunque muchos casos son asintomáticos, la infección puede manifestarse con diarrea y dolores musculares, siendo diagnosticada mediante análisis de heces o biopsias musculares. No existe un tratamiento específico, enfocándose la profilaxis en la cocción adecuada de las carnes y la higiene alimentaria. A nivel mundial, se han reportado casos, con mayor incidencia en ciertas regiones, y estudios en animales sugieren una exposición al riesgo en áreas como Venezuela. Se recomienda la realización de estudios serológicos en humanos para comprender mejor la exposición y alertar a los profesionales de la salud sobre esta parasitosis.
Puntos Clave:
- Definición y Etiología: La sarcocistosis (sinonimia: sarcosporidiosis) es una infección zoonótica causada por protozoarios coccidios del género Sarcocystis (anteriormente Isospora hominis). Es de importancia veterinaria y puede afectar tanto el tubo digestivo como los músculos de los humanos, causando diarrea y dolores musculares respectivamente.
- Ciclo de Vida y Hospedadores: El parásito tiene un ciclo de vida que involucra a hospedadores definitivos (carnívoros) donde se aloja en el tubo digestivo, y hospedadores intermediarios (herbívoros) donde se ubica en los músculos esqueléticos.
- Infección Humana: Los humanos pueden actuar como hospedadores definitivos e intermediarios.
- Infección Intestinal: Ocurre por la ingestión de carne cruda o mal cocida de vacunos (S. hominis) o porcinos (S. suihominis) infectados.
- Si bien estas son las fuentes principales mencionadas, se sugiere que una variedad más amplia de animales domésticos y silvestres (mamíferos y aves) podrían estar implicados. También se menciona un ciclo con primates no humanos como intermediarios y reptiles (ofidios) como definitivos (S. nesbitti) que podría involucrar al humano.
- Infección Muscular: Es más rara y se produce al ingerir esporoquistes presentes en alimentos contaminados con materia fecal de carnívoros o de humanos.
- Mecanismo de la Infección:
- Fase Intestinal: Los quistes liberan bradizoítos en el intestino, los cuales se transforman en gametos que, tras la conjugación, originan ooquistes. Estos ooquistes se liberan al intestino, se rompen y liberan esporoquistes maduros con cuatro esporozoítos cada uno.
- Fase Muscular: Los esporozoítos ingeridos se diseminan a través del endotelio vascular y células mononucleares hasta alcanzar la musculatura (estriada, cardíaca o lisa), donde se multiplican asexualmente (esquizogonia) formando quistes elongados que pueden alcanzar gran tamaño (hasta 300 μm o más). Generalmente, no hay reacción inflamatoria alrededor de estos quistes inicialmente.
- Manifestaciones Clínicas:
- Infección Intestinal: La mayoría de los casos son asintomáticos, pero puede causar un síndrome diarreico con dolor abdominal, náuseas, vómitos, escalofríos y sudoración, que aparece horas después de la ingesta. Los esporoquistes se detectan en las heces entre 1 y 2 semanas y su excreción puede persistir durante meses.
- Infección Muscular: Aunque la mayoría de los casos también son asintomáticos (descubiertos en biopsias o autopsias), la desintegración de los quistes puede provocar miositis con dolor muscular, fiebre, síntomas alérgicos, broncoespasmo, linfadenopatías, nódulos subcutáneos, eosinofilia y signos hematológicos de fase aguda y daño muscular (aumento de la eritrosedimentación, proteína C reactiva, LDH, AST, ALT y CK).
- Diagnóstico:
- Fase Entérica: Se realiza mediante el examen de heces, preferiblemente con métodos de flotación.
- Fase Muscular: Se diagnostica por biopsia de las zonas afectadas, teñidas con PAS.
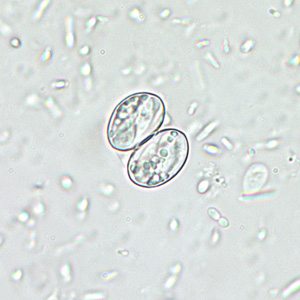
Ooquistes de Sarcocystis
Los ooquistes de Sarcocystis en las heces humanas miden 15-20 μm de largo por 15-20 μm de ancho. Los ooquistes esporulan en el epitelio intestinal y contienen dos esporocistos, cada uno de los cuales contiene cuatro esporozoítos y un cuerpo residual refractario. Debido a la naturaleza frágil de los ooquistes maduros, tanto los ooquistes esporulados como los esporocistos individuales pueden desprenderse en las heces. Los esporocistos se autofluorescen bajo microscopía ultravioleta (UV).
Sarcoquistes de Sarcocystis en tejido.
Solo se conocen dos especies de Sarcocystis que utilizan a los humanos como hospedador definitivo: S. hominis y S. suihominis. Los seres humanos se convierten en hospedadores intermediarios cuando ingieren los ooquistes de especies de Sarcocystis cuyos huéspedes definitivos son especies de mamíferos distintos de los humanos. Estas especies no humanas de Sarcocystis formarán estructuras conocidas como sarcoquistes en el tejido; Estos sarcoquistes contienen numerosos bradizoítos. Los sarcoquistes generalmente se encuentran en el músculo esquelético o cardíaco.
- Serología: Las pruebas de ELISA e inmunofluorescencia pueden ayudar a orientar la sospecha clínica y proporcionar datos epidemiológicos de exposición al riesgo.
- Tratamiento y Pronóstico: No existe un tratamiento específico ya que las infecciones intestinales y musculares son autolimitadas (la infección no se disemina a otras células) y no hay evidencia de tratamientos efectivos. Para la infección muscular, el uso de esteroides puede aliviar los síntomas.
- Profilaxis: La prevención se basa en la cocción adecuada de las carnes y el buen lavado de vegetales.
- Distribución Geográfica y Epidemiología: La sarcocistosis tiene una distribución mundial, aunque los reportes son escasos en Centro y Sudamérica, África y Medio Oriente. La distribución está relacionada con la cercanía del humano al ganado bovino y porcino, el consumo de carne cruda o poco cocida de estos animales y el acceso de estos animales a las heces humanas.
- Casos y Prevalencia: Históricamente, se han publicado alrededor de 100 casos individuales de sarcocistosis muscular, con más de la mitad provenientes de Malasia. Entre 2011 y 2014, se reportaron brotes y casos individuales, principalmente en turistas europeos que visitaron dos islas en Malasia, con aproximadamente 200 casos diagnosticados clínicamente como S. nesbitti (confirmado por PCR en músculo en algunos casos). En ese país, se ha detectado Sarcocystis en biopsias de lengua durante autopsias con una frecuencia cercana al 21%. Se estima que se han reportado más de 2.000 infecciones humanas sintomáticas (intestinal y muscular) en todo el mundo. La prevalencia de sarcocistosis intestinal se ha estimado entre 1,1% y 10,4% en Europa, y entre 0,4% y 23,2% en Asia. La prevalencia de la sarcocistosis muscular se estima entre 0% y 3,6% en países occidentales industrializados.
- Situación en Venezuela: No se encontró información sobre la frecuencia de sarcocistosis en humanos en Venezuela. Sin embargo, se encontraron altas prevalencias de infección por Sarcocystis en animales de producción: 92,8% en corazones de vacunos de Bolívar (1977), 98% en búfalos de agua sacrificados en Barquisimeto (2016) y entre 1% y 11,5% en cerdos de Lara (2005). Esto sugiere una exposición al riesgo de infección importante en el país.
- Recomendaciones: Dada la alta prevalencia de Sarcocystis en animales de producción en Venezuela, se considera prudente realizar encuestas serológicas en la población para determinar el nivel de exposición al riesgo. Además, se recomienda alertar a médicos y bioanalistas sobre la posibilidad de incluir esta parasitosis en el diagnóstico clínico y de laboratorio de patologías musculares y diarreicas.
Preguntas sobre Sarcocistosis
- ¿Qué es la sarcocistosis y cuáles son sus principales manifestaciones en humanos?
- La sarcocistosis, también conocida como sarcosporidiosis, es una infección zoonótica causada por parásitos protozoarios coccidios del género Sarcocystis. En humanos, se manifiesta principalmente de dos formas: la forma intestinal, que suele ser asintomática pero puede causar un síndrome diarreico con dolor abdominal, náuseas, vómitos, escalofríos y sudoración tras la ingesta; y la forma muscular, que en la mayoría de los casos es asintomática y se detecta en biopsias o autopsias, pero que al desintegrarse los quistes puede provocar miositis con dolor muscular, fiebre, síntomas alérgicos, broncoespasmo, entre otros síntomas.
- ¿Cómo se transmite la sarcocistosis en humanos?
- La transmisión de la sarcocistosis en humanos ocurre de dos maneras principales. La forma intestinal se adquiere al ingerir carne cruda o mal cocida de animales infectados, principalmente vacunos (S. hominis) o porcinos (S. suihominis). La forma muscular, aunque menos frecuente, se produce al ingerir esporoquistes presentes en alimentos contaminados con materia fecal de carnívoros o de otros humanos que albergan el parásito en su intestino. También se ha descrito un ciclo que involucra primates no humanos como hospedadores intermediarios y reptiles como hospedadores definitivos (S. nesbitti), donde el humano podría también infectarse.
- ¿Cuál es el ciclo de vida del parásito Sarcocystis y qué papel juegan los diferentes hospedadores?
- El ciclo de vida de Sarcocystis involucra dos tipos de hospedadores: definitivos y intermediarios. Los carnívoros actúan como hospedadores definitivos, albergando las formas adultas del parásito en su tubo digestivo, donde se reproducen sexualmente y liberan esporoquistes en las heces. Los herbívoros son los hospedadores intermediarios, en cuyos músculos esqueléticos se desarrollan quistes (sarcosporidios) llenos de bradizoítos después de la ingestión de los esporoquistes. Los humanos pueden actuar como ambos tipos de hospedadores, adquiriendo la forma intestinal al consumir carne infectada y la forma muscular al ingerir esporoquistes.
- ¿Cómo se diagnostica la sarcocistosis en humanos?
- El diagnóstico de la sarcocistosis en la fase intestinal se realiza mediante el examen de las heces, preferiblemente utilizando métodos de flotación para identificar los esporoquistes. La fase muscular se diagnostica mediante la biopsia de las zonas musculares afectadas, donde se pueden observar los quistes al teñir las muestras con PAS. Las pruebas serológicas como ELISA e inmunofluorescencia pueden ayudar a orientar el diagnóstico y proporcionar datos epidemiológicos sobre la exposición al parásito.
- ¿Existe un tratamiento específico para la sarcocistosis humana?
- Actualmente, no existe un tratamiento específico para la sarcocistosis humana, ya que tanto las infecciones intestinales como musculares son autolimitadas. No hay evidencia de tratamientos que eliminen la infección. Para la infección muscular sintomática, se ha observado que el uso de esteroides puede mejorar los síntomas asociados a la miositis.
- ¿Cuáles son las medidas de prevención recomendadas para evitar la sarcocistosis?
- La profilaxis de la sarcocistosis se basa principalmente en dos medidas: la cocción adecuada de las carnes de consumo, especialmente de vacuno y porcino, a temperaturas que aseguren la muerte de los parásitos, y el lavado minucioso de vegetales que puedan haber estado en contacto con heces contaminadas.
- ¿Cuál es la distribución geográfica de la sarcocistosis y qué factores influyen en su prevalencia?
- La sarcocistosis tiene una distribución mundial, aunque se han reportado menos casos en Centro y Sudamérica, África y Medio Oriente. La prevalencia está influenciada por la cercanía de los humanos al ganado bovino y porcino, las costumbres de consumir carne cruda o poco cocida de estos animales y el acceso de estos animales a heces humanas. Estudios han mostrado una prevalencia variable en diferentes regiones de Europa y Asia para la forma intestinal, y una prevalencia generalmente baja en países occidentales industrializados para la forma muscular. En Venezuela, aunque no hay datos específicos en humanos, la alta prevalencia en animales de consumo sugiere una importante exposición al riesgo.
- ¿Qué implicaciones tienen los hallazgos de sarcocistosis en animales para la salud humana y qué se recomienda en el contexto de Venezuela?
- La alta prevalencia de Sarcocystis encontrada en el corazón de vacunos, búfalos de agua y cerdos en diferentes regiones de Venezuela sugiere que la población humana podría estar expuesta al riesgo de infección. Ante la falta de información sobre la frecuencia de sarcocistosis en humanos en el país, se recomienda realizar encuestas serológicas para determinar el nivel de exposición al riesgo. Además, es importante alertar a médicos y bioanalistas sobre la posibilidad de incluir esta parasitosis en el diagnóstico diferencial de patologías musculares y diarreicas, considerando los hallazgos en animales como un indicador de potencial riesgo para la salud pública.
Autoevaluación
Centers for Disease Control and Prevention. (s.f.). DPDx - Sarcocystosis. Recuperado el 4 de abril de 2025, de
Parasitología Aula Virtual. (s.f.). Sarcocistosis [Playlist]. YouTube. https://www.youtube.com/playlist?list=PLUacIHFf9ZXZeSOBjaNHTzcpmh79Oy605







Comentarios
Publicar un comentario