AMEBAS DE VIDA LIBRE (Naegleria, Acanthamoeba, Balamuthia).
Podcast
Videos
Resumen
El texto describe las infecciones ocasionadas por amibas de vida libre, organismos ubicuos que pueden volverse parasitarios en humanos, causando patologías severas como la meningoencefalitis primaria amibiana (MPA), la encefalitis granulomatosa amibiana (EGA) y la queratitis amibiana (QA). Se detallan los agentes causales, principalmente de los géneros Naegleria, Acanthamoeba, y la especie Balamuthia mandrillaris, así como sus características morfológicas, ciclos de vida y los mecanismos de infección. Además, el documento aborda la sintomatología, los métodos de diagnóstico que incluyen análisis de fluidos, biopsias e imagenología, y las opciones de tratamiento, que suelen ser limitadas con altas tasas de mortalidad, junto con algunas medidas de prevención específicas para la queratitis amibiana. Finalmente, se proporciona un panorama de la epidemiología global y específicamente en Venezuela, resaltando la rareza de estas infecciones y la importancia del reporte de casos.
Temas Principales y Puntos Clave
La fuente describe tres principales patologías humanas atribuidas a amibas de vida libre, que son microorganismos habitualmente presentes en la naturaleza pero que pueden volverse parasitarios en ciertas condiciones:
- Meningoencefalitis Primaria Amibiana (MPA): Causada por especies del género Naegleria, principalmente N. fowleri.
- Encefalitis Granulomatosa Amibiana (EGA): Causada principalmente por especies del género Acanthamoeba y por Balamuthia mandrillaris.
- Queratitis Amibiana (QA): Causada por especies del género Acanthamoeba.
Características Generales de las Amibas de Vida Libre:
- Son ubicuas, encontrándose en diversos ambientes como suelo, agua (natural y artificial), aire e incluso en las mucosas de individuos sanos.
- Tienen un ciclo de vida libre en la naturaleza.
- Son parásitos facultativos, es decir, pueden vivir independientemente pero pueden infectar a humanos y animales bajo ciertas circunstancias.
- La transmisión entre personas es rara y solo ocurre en casos de trasplante de órganos.
1. Naegleriasis
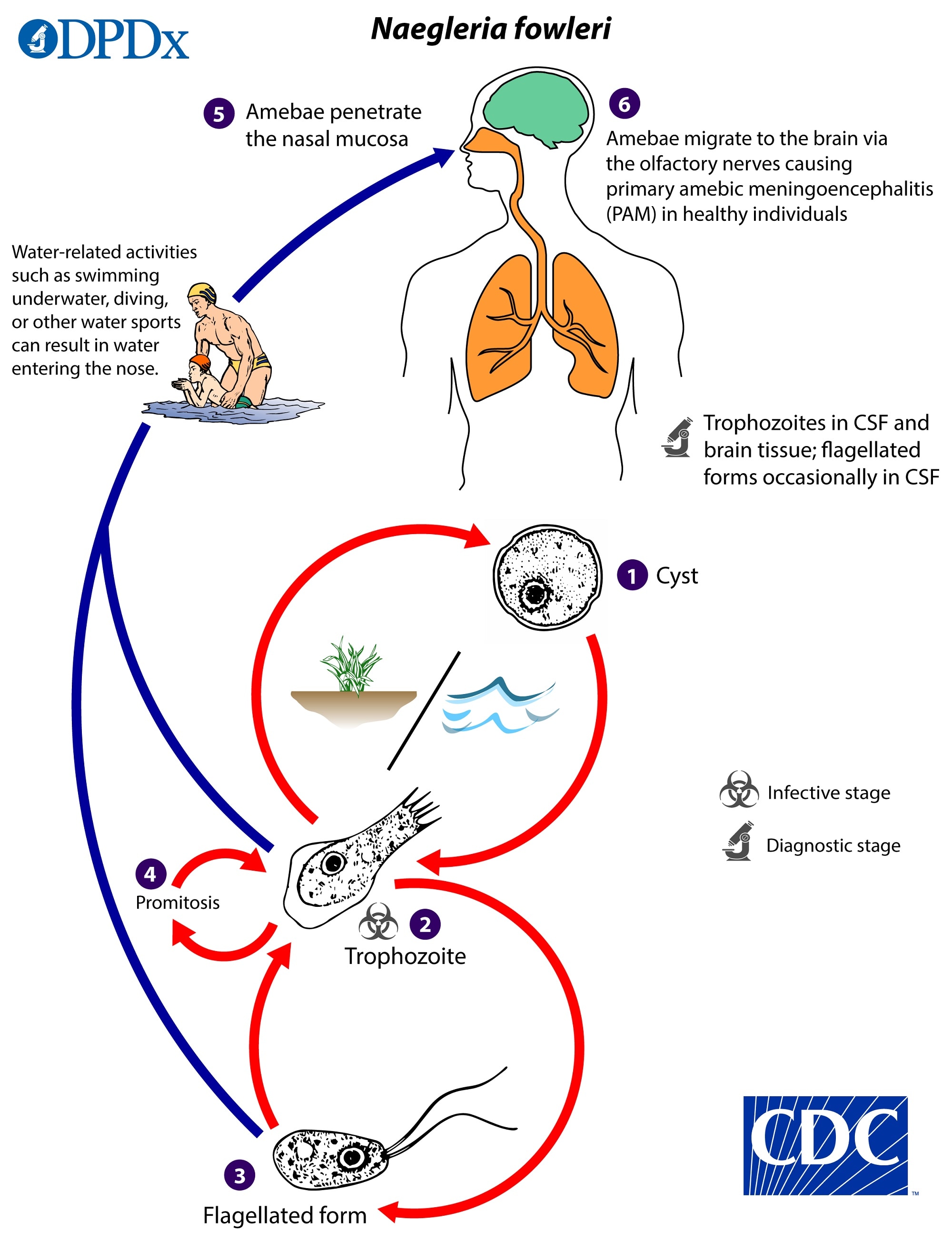
- Infección: Infección del sistema nervioso central causada por Naegleria fowleri, denominada Meningoencefalitis Amibiana Primaria (MAP).
- Características: Curso rápido y frecuentemente mortal, que ocurre en niños y adultos jóvenes sanos.
- Morfología:
- Trofozoíto: 10-30 µm, con una forma flagelada transitoria en agua destilada.
- Quiste: Esférico de 10 µm con una sola capa.
- Hábitat: Parásito termófilo, encontrado en ecosistemas acuáticos de temperaturas tibias (hasta 45°C), como lagos cálidos en verano, piscinas y aguas de plantas termoeléctricas.
- Epidemiología: Afecta a personas sanas (a diferencia de Acanthamoeba), con más casos en niños varones. Importante número de casos en Australia y USA. La seroprevalencia es mucho mayor que la casuística.
- Patogenia: Penetración a través de la membrana olfatoria, hacia el nervio olfatorio, espacio subaracnoideo y cerebro.
- Patología: Lesiones necróticas, hemorrágicas e inflamatorias purulentas en corteza cerebral y meninges, similar a una meningitis bacteriana pero "estéril".
- Síntomas: Curso agudo y fulminante con incubación corta (días a 2 semanas). Comienza con distorsión del olfato y gusto, evoluciona a meningoencefalitis aguda, coma y muerte en 1 semana.
- Diagnóstico: A diferencia de Acanthamoeba, se detectan trofozoítos en el líquido cefalorraquídeo (LCR) y en los tejidos. El LCR es purulento pero sin bacterias al Gram. Se prefiere la visualización al fresco. Tinciones con calcoflúor, inmunofluorescencia, inmunohistoquímica y detección molecular son útiles. También el cultivo en agar con E. coli.
Quistes de Naegleria fowleri.
Naegleria fowleri no forma quistes en el tejido humano. Los quistes en el medio ambiente y el cultivo son esféricos, de 7 a 15 μm de diámetro y tienen una pared lisa de una sola capa. Los quistes tienen un solo núcleo.
Trofozoítos de Naegleria fowleri.
Hay dos formas de trofozoítos en Naegleria fowleri: ameboide y ameboflagelado, el último de los cuales solo se encuentra raramente en humanos (dentro del LCR). Los trofozoítos ameboides miden entre 10 y 35 μm, pero cuando se redondean suelen tener entre 10 y 15 μm de diámetro. En cultivo, los trofozoítos pueden crecer hasta más de 40 μm. El citoplasma es granular y contiene muchas vacuolas. El núcleo único es grande y tiene un carioma grande y denso y carece de cromatina periférica.
- Tratamiento: Muy limitado, con más del 95% de mortalidad. Algunos sobrevivientes han recibido anfotericina B IV a altas dosis (incluyendo intratecal) con terapia adyuvante de rifampicina, miconazol y sulfisoxazol. Combinaciones experimentales promisorias incluyen anfotericina, miltefosina y clorpromazina.
2. Acantamebiasis
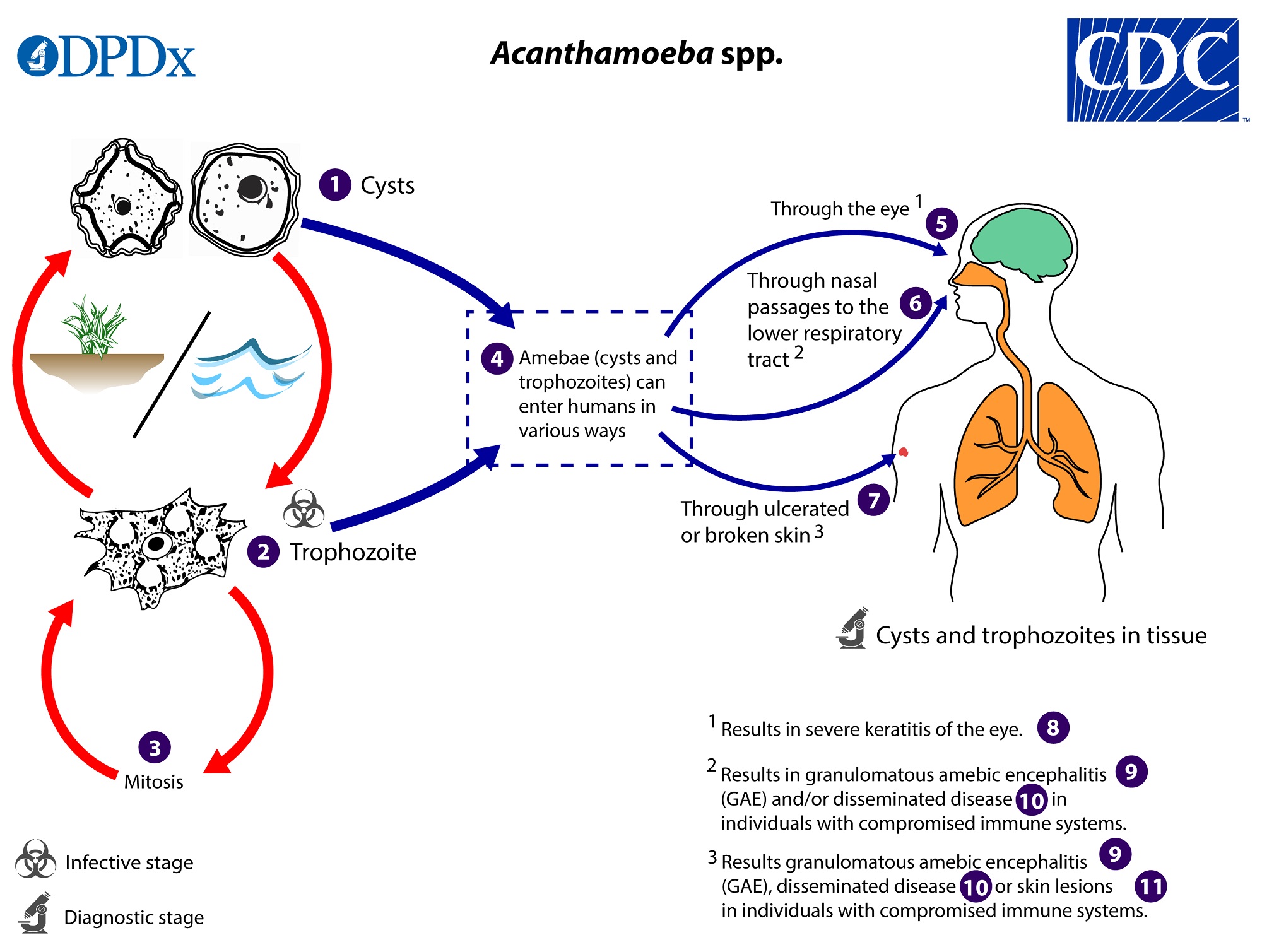
- Infección: Afecta el sistema nervioso central (EGA), la piel y la córnea (QA).
- Agente Causal: Diversas especies del género Acanthamoeba (se listan 11 especies).
- Morfología: Presenta dos formas:
- Trofozoíto: Forma vegetativa de 20 a 40 µm con proyecciones finas llamadas acantopodios.
- Quiste: Forma de resistencia poliédrica de unos 15 µm con dos paredes (externa irregular e interna redondeada).
- "Ambos, trofozoítos y quistes, se pueden encontrar en los tejidos y en la naturaleza."
- Patogenia:
- EGA: La entrada parece ser por lesiones en la piel, vía respiratoria o genitourinaria, con diseminación al SNC por vía hematógena.
- QA: Habitualmente por manejo poco higiénico de lentes de contacto, aunque se han dado casos sin este antecedente.
- Susceptibilidad: Todos los grupos etarios son susceptibles, pero la amiba invade preferentemente individuos debilitados o con inmunodeficiencias.
- Síntomas:
- EGA: Cefalalgia, trastornos motores, sensoriales, mentales y meníngeos. Indistinguible de la causada por Balamuthia. Puede diseminarse a otros órganos.
- Ojo (QA): Queratitis, úlceras corneales crónicas y uveítis.
- Piel: Lesiones papulonodulares que pueden ulcerarse, en tronco y extremidades.
- Diagnóstico:
- SNC (EGA): Imagenología encefálica (múltiples lesiones), biopsia de las lesiones (estudio morfológico, inmunológico, inmunohistoquímico y molecular), cultivo de las lesiones en agar con E. coli. Los parásitos no se detectan en LCR.
- Piel: Similar al SNC, mediante biopsia y cultivo.
- QA: Examen del raspado corneal al fresco o teñido (Giemsa o calcoflúor). También se pueden examinar los lentes de contacto y su material de almacenamiento.
Quistes de Acanthamoeba spp.
Los quistes de Acanthamoeba spp. suelen tener entre 10 y 25 μm de diámetro. Los quistes tienen una pared de dos capas con poros: una pared externa fibrosa arrugada (exoquiste) y una pared interna (endoquiste) que puede ser hexagonal, esférica, en forma de estrella o poligonal. Los quistes contienen un solo núcleo con un carioma grande. Los quistes se pueden encontrar en el cerebro, los ojos, la piel, los pulmones y otros órganos.
Trofozoítos de Acanthamoeba spp.
Los trofozoítos de Acanthamoeba spp. son pleomórficos y miden aproximadamente 15-45 μm. A menudo tienen múltiples procesos similares a la columna vertebral llamados acantapodia. Los trofozoítos contienen un núcleo grande con un carioma grande ubicado en el centro, pero no cromatina periférica. No hay estadio de trofozoíto flagelado en Acanthamoeba spp.
- Tratamiento: Se han ensayado combinaciones de diversos fármacos como pentamidina, itraconazol, fluconazol, ketoconazol, hydroxystilbamidina, paromomicina, 5-fluorocitosina, polimixina, sulfadiazina, trimetoprim-sulfametoxazol y azitromicina. Para lesiones cutáneas, itraconazol, pentamidina y 5-fluorocitosina con terapia tópica de clorhexidina y ketoconazol. Lesiones corneales con antisépticos catiónicos (clorhexidina, poliheximetileno biguanida, hexamidina) combinados con tratamiento sistémico (propamidina, neomicina) por períodos prolongados.
- Pronóstico: La mortalidad de los casos cutáneos combinados con EGA es casi del 100%.
- Epidemiología y Control: No existen medidas particulares de control para la EGA. Para la QA, se recomienda la higiene adecuada de los lentes de contacto y evitar su uso al nadar. No tiene distribución geográfica particular.
3. Balamutiasis
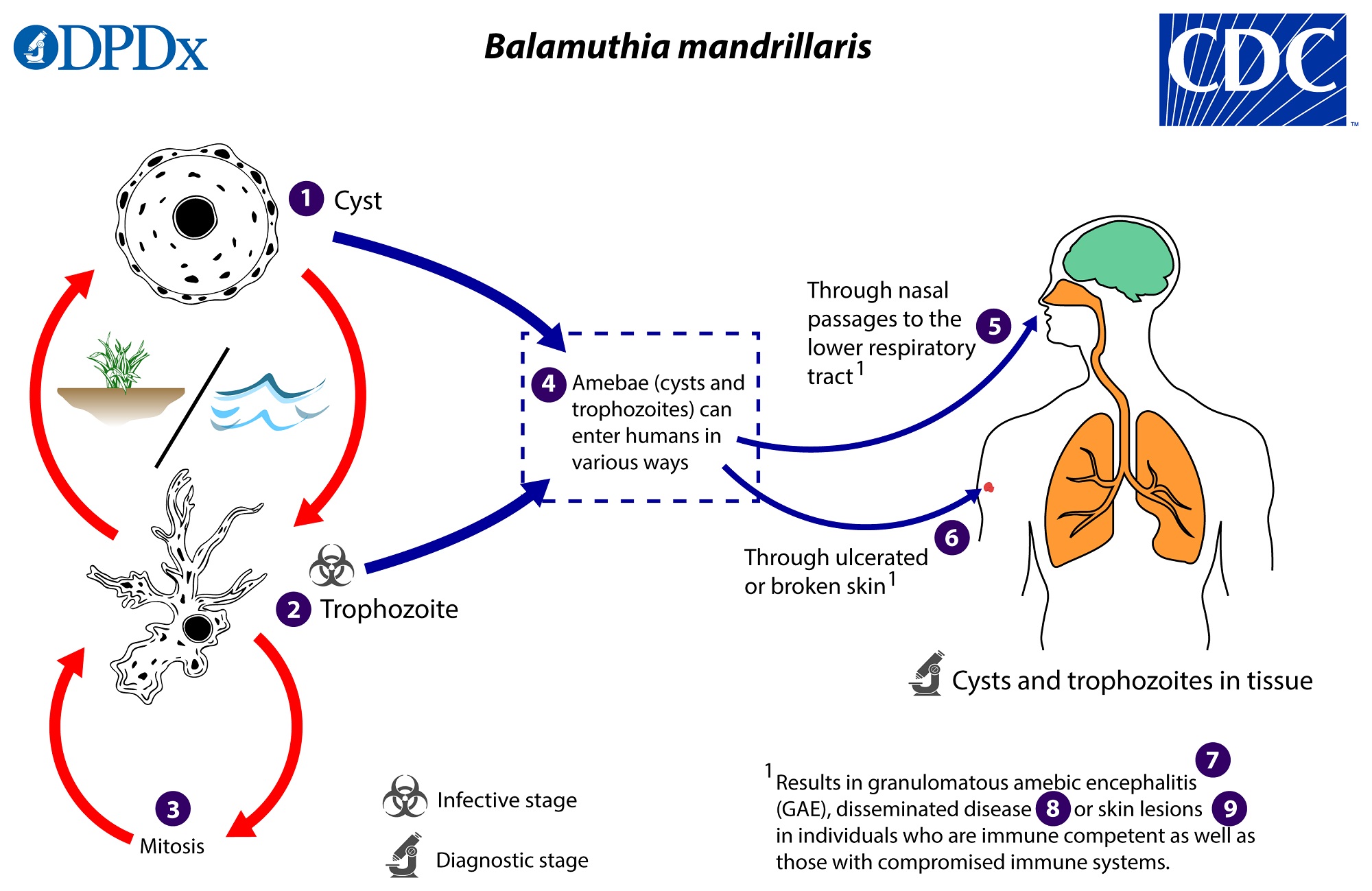
- Infección: Infección del sistema nervioso central causada por Balamuthia mandrillaris, resultando en Encefalitis Granulomatosa Amibiana (EGA), similar a la causada por Acanthamoeba.
- Morfología:
- Trofozoíto: Muy pleomórfico, con proyecciones gruesas irregulares, de 12 a 60 µm.
- Quiste: Redondeado de 12 a 30 µm con dos paredes (externa irregular e interna redondeada), similar a Acanthamoeba.
- Transmisión: Por penetración del trofozoíto a través de pequeñas heridas en la piel o por aspiración nasal o bucal, alcanzando el SNC posiblemente por vía hematógena. Causa lesiones de piel en la puerta de entrada.
- Incubación y Duración: De semanas a meses. No se transmite de persona a persona (salvo trasplante de órganos).
- Síntomas: Clínica similar a Acanthamoeba. Lesiones de piel (no dolorosas, tipo placas) en la parte central de la cara, tronco y rodillas, que pueden preceder a la sintomatología neurológica por meses o años. Puede haber diseminación a varios órganos.
- Diagnóstico: Detección de anticuerpos específicos marcados por inmunofluorescencia o inmunohistoquímica y detección molecular (PCR) en biopsias de piel o cerebro. El LCR muestra linfocitosis importante y ligera elevación de proteínas, pero el parásito no se encuentra habitualmente. No crece en agar con E. coli, sino en monocapas de tejidos de mamífero.
Quistes de Balamuthia mandrillaris.
Los quistes de Balamuthia mandrillaris son muy similares morfológicamente a los de Acanthamoeba spp. y también suelen tener entre 10 y 25 μm (una media de 15 μm) de diámetro. Por lo general, no se pueden distinguir de manera confiable de Acanthamoeba spp. sin confirmación molecular o microscopía electrónica. Los quistes tienen dos paredes aparentes en la microscopía óptica y no tienen poros: una pared externa fibrosa arrugada (exoquiste) y una pared interna (endoquiste) que puede ser de forma variable. Una tercera capa (mesocisto) solo es visible a través de la microscopía electrónica. Los quistes contienen un solo núcleo con un carioma grande. Los quistes se pueden encontrar en el cerebro, la piel, los pulmones y otros órganos.
Balamuthia mandrillaris trofozoítos.
Los trofozoítos de Balamuthia mandrillaris son pleomórficos y miden aproximadamente 15-60 μm. A menudo producen seudópodos largos (más anchos que los de Acanthamoeba spp.). Los trofozoítos contienen un núcleo grande con un carioma grande ubicado en el centro, pero no cromatina periférica. Las formas binucleadas son raras. No hay estadio de trofozoíto flagelado en B. mandrillaris.
- Pronóstico: Malo, con cerca del 95% de mortalidad.
- "El pronóstico es malo y cerca del 95% fallecen: de poco más de 150 casos diagnosticados para el 2010, solo 7 habían sobrevivido."
- Tratamiento: En sobrevivientes se han utilizado combinaciones de pentamidina, sulfadiazina, azitromicina/claritromicina, flucitosina y fluconazol. Recientemente se reporta éxito con la adición de miltefosina y albendazol.
- Epidemiología y Control: Afecta a personas de cualquier edad, con predilección por los extremos etarios y personas en buen estado de salud, pero con mayor riesgo en inmunodeficientes. Descrito en todos los continentes excepto África, con mayoría de casos en Norte y Sudamérica (en Norteamérica, más frecuente en la población hispánica). La prevención es difícil por la escasa casuística y dificultad para identificar factores de riesgo específicos. Se recomienda evitar baños en aguas donde se han detectado casos.
Situación en Venezuela:
- Los primeros casos publicados de MAP y EGA (sin diagnóstico etiológico en este último) datan de 1980.
- El primer diagnóstico de EGA por B. mandrillaris fue en 1991.
- Un caso de EGA por Acanthamoeba spp. se reportó en 2011.
- Los primeros reportes de QA y conjuntivitis amibiana fueron en 1993.
- Un diagnóstico molecular retrospectivo de infección por Acanthamoeba en 18 de 550 muestras humanas (aisladas entre 1984 y 2014 de lesiones sospechosas) se publicó en 2016.
Conclusión:
La fuente proporciona una visión general detallada de las amibiasis por amibas de vida libre, destacando sus diferencias en cuanto a agente etiológico, patogenia, presentación clínica, diagnóstico y tratamiento. Subraya la gravedad de las infecciones del SNC como la MPA y la EGA, con altas tasas de mortalidad, y la importancia de la higiene en la prevención de la QA. La información sobre la casuística en Venezuela resalta la presencia de estas infecciones en el país, aunque con una frecuencia limitada. La dificultad en el diagnóstico y tratamiento, especialmente de las infecciones del SNC, enfatiza la necesidad de una mayor investigación y concienciación sobre estas enfermedades parasitarias.
Imágenes de patología macroscópica en infecciones amebianas de vida libre.
Muestras de tejido macroscópico y patología de infecciones amebianas de vida libre.
Muestra macroscópica de tejido cerebral de un paciente que murió de encefalitis amebiana granulomatosa (GAE) causada por Balamuthia mandrillaris. El espécimen de la autopsia reveló una extensa encefalitis granulomatosa necrotizante (mixta inflamatoria, células gigantes ocasionales, vasculítica) con un proceso necroinflamatorio subependimario. Imagen cortesía de Cook Children's Hospital, Fort Worth, Texas.
Preguntas sobre Amibiasis por Amibas de Vida Libre
¿Qué son las amibas de vida libre y cómo pueden causar enfermedades en humanos?
Las amibas de vida libre son un grupo de protozoarios ubicuos que normalmente existen en la naturaleza (suelo, agua dulce y artificial, aire) y no requieren un huésped para completar su ciclo de vida. Sin embargo, bajo ciertas condiciones, algunas especies pueden volverse parásitas accidentales en humanos, causando infecciones graves como la meningoencefalitis primaria amibiana (MPA), la encefalitis granulomatosa amibiana (EGA) y la queratitis amibiana (QA).
¿Cuáles son las principales enfermedades causadas por amibas de vida libre mencionadas en el texto y qué géneros de amibas están asociados a cada una?
Las principales enfermedades mencionadas son:
- Meningoencefalitis Primaria Amibiana (MPA): Causada principalmente por especies del género Naegleria (hasta ahora solo N. fowleri).
- Encefalitis Granulomatosa Amibiana (EGA): Causada por especies del género Acanthamoeba y por la especie Balamuthia mandrillaris.
- Queratitis Amibiana (QA): Causada por especies del género Acanthamoeba.
¿Cómo se contraen típicamente la Meningoencefalitis Primaria Amibiana (MPA) y qué la diferencia de la Encefalitis Granulomatosa Amibiana (EGA)?
La MPA causada por Naegleria fowleri se contrae cuando agua contaminada que contiene los trofozoítos de la amiba entra por la nariz, viaja a través del nervio olfatorio hasta el cerebro, causando una infección rápida y a menudo mortal. A diferencia de la EGA, la MPA suele afectar a niños y adultos jóvenes sanos y tiene un curso clínico agudo y fulminante con un periodo de incubación corto. Además, en la MPA se detectan trofozoítos en el líquido cefalorraquídeo (LCR), lo cual no es común en la EGA.
¿Cuáles son las vías de entrada y los factores de riesgo para la Encefalitis Granulomatosa Amibiana (EGA) causada por Acanthamoeba y Balamuthia mandrillaris?
Para la EGA causada por Acanthamoeba, las vías de entrada parecen ser lesiones en la piel, la vía respiratoria o genitourinaria, con diseminación al sistema nervioso central por vía hematógena. La EGA por Balamuthia mandrillaris puede ocurrir por la penetración de trofozoítos a través de pequeñas heridas en la piel o por aspiración nasal o bucal. Si bien todos los grupos etarios son susceptibles a las infecciones por Acanthamoeba, la EGA por Balamuthia parece tener una predilección por los extremos etarios y las personas con algún nivel de inmunodeficiencia.
¿Cómo se manifiesta clínicamente la Queratitis Amibiana (QA) y cuál es el factor de riesgo más común para su desarrollo?
La Queratitis Amibiana se manifiesta como una inflamación de la córnea y puede causar úlceras corneales crónicas y, en algunos casos, uveítis. El factor de riesgo más común para su desarrollo es el manejo poco higiénico de lentes de contacto, aunque también se han reportado casos en personas que no usan lentes de contacto.
¿Cuáles son los métodos de diagnóstico para las infecciones por amibas de vida libre como MPA, EGA y QA?
El diagnóstico de la MPA se realiza mediante la detección de trofozoítos de Naegleria fowleri en el LCR mediante observación al fresco, tinciones especiales (calcoflúor), inmunofluorescencia, inmunohistoquímica o detección molecular. Para la EGA, causada por Acanthamoeba o Balamuthia, el diagnóstico se basa en la biopsia de las lesiones cerebrales o de piel, seguida de estudios morfológicos, inmunológicos (con anticuerpos específicos), inmunohistoquímicos y moleculares (PCR). En la EGA por Balamuthia, el LCR puede mostrar linfocitosis y elevación de proteínas, aunque el parásito no se detecta habitualmente en él. La QA se diagnostica mediante el examen del raspado corneal al fresco o teñido, y también se pueden examinar los lentes de contacto y sus estuches.
¿Qué tan efectivas son las opciones de tratamiento para las infecciones por amibas de vida libre y cuál es el pronóstico general?
El tratamiento para las infecciones por amibas de vida libre es desafiante y a menudo tiene un pronóstico desfavorable. La MPA causada por Naegleria fowleri tiene una tasa de mortalidad superior al 95%, aunque algunos sobrevivientes han sido tratados con anfotericina B a altas dosis (incluyendo intratecal) combinada con otros medicamentos. La EGA por Acanthamoeba y Balamuthia también tiene una alta mortalidad, cercana al 95%. Los tratamientos ensayados incluyen combinaciones de varios antifúngicos y antibióticos, y en algunos casos de EGA por Balamuthia, se ha reportado éxito con la adición de miltefosina y albendazol. La QA tiene mejores perspectivas de tratamiento con agentes antisépticos tópicos y, en algunos casos, medicamentos sistémicos.
¿Qué medidas de prevención se recomiendan para evitar las infecciones por amibas de vida libre?
Para la MPA, se recomienda evitar nadar o sumergirse en aguas dulces templadas y estancadas, especialmente durante los meses cálidos, o usar pinzas nasales si se hace. Para la QA, es crucial mantener una higiene rigurosa de los lentes de contacto, utilizando soluciones de limpieza y almacenamiento adecuadas (solución salina esterilizada con calor o con benzilconio) y evitar usarlos al nadar. Para la EGA, la prevención es más difícil debido a la ubicuidad de las amibas y la falta de factores de riesgo específicos claramente definidos, aunque se recomienda evitar baños en cuerpos de agua donde se han detectado casos. En general, para todas las infecciones por amibas de vida libre del SNC y piel, la prevención sigue siendo un desafío debido a la baja frecuencia de casos y la dificultad para identificar riesgos específicos.
Autoevaluación
Bibliografía
Centers for Disease Control and Prevention. (s.f.). DPDx - Free Living Amebic Infections. Recuperado el 4 de abril de 2025, de
Parasitología Aula Virtual. (s.f.). Amebas de Vida Libre [Playlist]. YouTube. https://www.youtube.com/playlist?list=PLUacIHFf9ZXZCHLzYozlDImkBrvvRLZyJ
Parasitología Aula Virtual. (s.f.). Naegleriasis [Playlist]. YouTube. https://www.youtube.com/playlist?list=PLUacIHFf9ZXaT7em6zrgaqexuj2LpKlNw
Parasitología Aula Virtual. (s.f.). Acantamebiasis [Playlist]. YouTube. https://www.youtube.com/playlist?list=PLUacIHFf9ZXYPkDa_zD080ydSTJY2D7Ku
Parasitología Aula Virtual. (s.f.). Balamutiasis [Playlist]. YouTube. https://www.youtube.com/playlist?list=PLUacIHFf9ZXbpR9rV_oKpGTp8GCArgBgs












Comentarios
Publicar un comentario