TRIPANOSOMIASIS AMERICANA (Enfermedad de Chagas)
Podcast
Videos
Resumen
Este documento informativo presenta un análisis de la Enfermedad de Chagas, una afección parasitaria crónica causada por Trypanosoma cruzi, considerada una enfermedad desatendida con fuerte vinculación a condiciones socioeconómicas deficitarias. La enfermedad es endémica en 21 países de las Américas, con potencial de propagación a países no endémicos a través de la migración. La transmisión principal es vectorial a través de insectos triatominos hematófagos ("chinches"), aunque también puede ocurrir por transfusión, vía congénita, trasplantes de órganos y oral. La enfermedad tiene una fase aguda, a menudo asintomática, y una fase crónica que puede desarrollar daños irreversibles en el corazón, el sistema digestivo y el sistema nervioso. El diagnóstico varía según la fase y el tratamiento con Benznidazol y Nifurtimox es efectivo, especialmente en etapas tempranas. A pesar de los avances significativos en el control vectorial y tamizaje sanguíneo en las Américas, persisten desafíos relacionados con la migración, la sostenibilidad de los programas y la necesidad de ampliar el acceso al diagnóstico y tratamiento.
Temas Principales y Puntos Clave:
1. Definición y Agente Causal:
- La Enfermedad de Chagas, o tripanosomiasis americana, es una afección parasitaria, sistémica, crónica causada por el protozoario Trypanosoma cruzi.
- Afecta principalmente la musculatura cardíaca, estriada y lisa, el sistema nervioso y el sistema macrofágico histiocitario.
- Tiene una firme vinculación con aspectos socioeconómico-culturales deficitarios, siendo considerada una enfermedad desatendida.
- Es una patología endémica en 21 países de las Américas.
- La distribución natural del parásito y su transmisión vectorial es exclusiva del continente americano, pero la migración ha llevado la infección a otros países.
2. Modos de Transmisión:
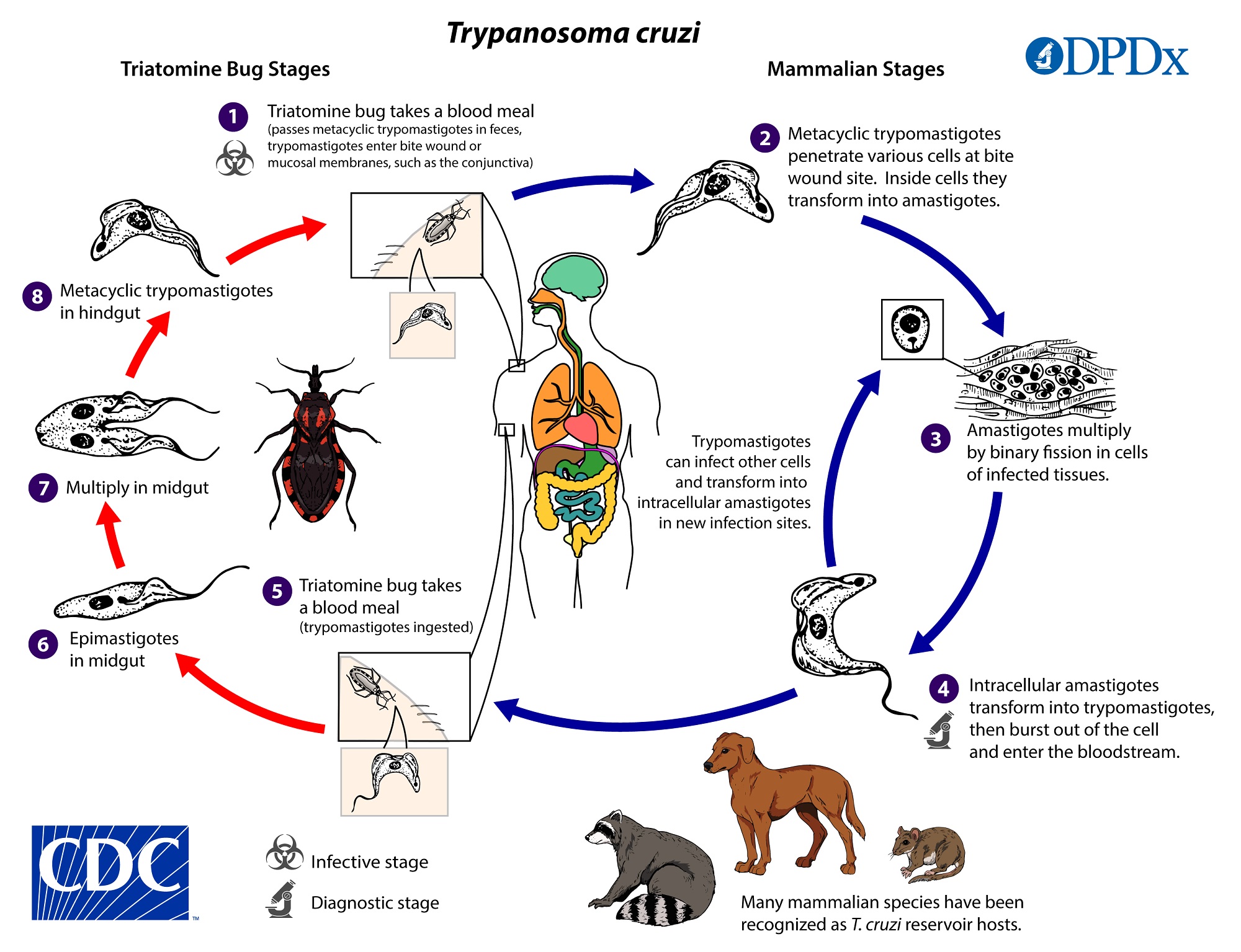
- Vectorial: Principal mecanismo, a través de hemípteros (chinches) de la subfamilia Triatominae. Estos insectos se alimentan de sangre y depositan sus heces infectadas con T. cruzi en heridas de la piel o sobre mucosas después de picar.
- El parásito entra al cuerpo cuando la persona se rasca instintivamente y contamina la picadura, ojos o boca.
- Los vectores viven mayoritariamente en las Américas, a menudo en grietas y ranuras de viviendas mal construidas en zonas rurales o suburbanas.
- Vectores importantes incluyen: Triatoma infestans, R. prolixus, T. dimidiata y Rhodnius pallescen
- Insecto triatomino, vector de Trypanosoma cruzi.
- https://www.cdc.gov/dpdx/trypanosomiasisamerican/index.html
- No Vectorial:
- Transfusional: Transmisión a través de sangre donada infectada (Incani (2020) menciona 10-25% de las unidades infectadas).
- Congénita: Transmisión vertical de la madre infectada al hijo durante el embarazo (OPS/OMS menciona 1% de los casos, Incani (2020) cerca del 5% de las madres infectadas).
- Trasplantes de órganos: Receptores de órganos de donantes infectados.
- Oral: Ingestión accidental de alimentos contaminados con T. cruzi, a menudo por heces de vectores o vectores completos. Incani (2020) destaca la importancia creciente de esta vía, habiendo causado microepidemias.
- Transmisión por lactancia materna es controversial (Incani, 2020).
- Infección accidental de laboratorio.
3. Reservorios y Fuente de Infección:
- La tripanosomiasis americana es una enzoosis de mamíferos silvestres, siendo el humano un hospedador accidental.
- Un número abundante de especies de mamíferos silvestres pueden estar infectados (cerca de 180 especies).
- Reservorios importantes que acercan la infección a la vivienda humana incluyen armadillos, rabipelados (zarigüellas), roedores domésticos (rata y ratón) y animales domésticos como perros y gatos.
- Las aves no son reservorios pero sirven de fuente de alimentación para los vectores.
- La cercanía de la vivienda a ecosistemas de transmisión enzoótica, como palmeras utilizadas para techos, es importante.
- Los ciclos silvestres y domésticos están interconectados, e incluso el ciclo silvestre puede darse en áreas urbanizadas con reservorios, vectores y ecosistemas apropiados.
4. Fases Clínicas de la Enfermedad:
La enfermedad tiene tres etapas:
- Fase Aguda:
- Dura pocas semanas después de la infección.
- Alto número de parásitos circulan en la sangre.
- Puede ser asintomática o presentar síntomas leves.
- Signos y síntomas:
- Chagoma de inoculación: Lesión cutánea en el sitio de la picadura (nódulo o placa, blando e indoloro).
- Signo de Romaña: Edema palpebral unilateral con adenopatías satélites (típico pero poco frecuente, 2% de los casos agudos sintomáticos).
- Fiebre, dolor de cabeza.
- Náuseas, diarrea o vómitos.
- Ganglios linfáticos agrandados.
- Dificultad para respirar.
- Dolor muscular, abdominal o en el pecho.
- En la fase aguda, los parásitos se reproducen intensamente en diversos tejidos, destruyendo células y causando inflamación.
- La meningoencefalitis y la pancarditis pueden ser fatales en individuos inmunodeprimidos durante esta fase.
- Fase de Latencia o Crónica Indeterminada:
- Se inicia después de la fase aguda y puede durar varios años o décadas.
- Muchas personas (70-80% de los infectados) son asintomáticas toda su vida.
- La parasitemia es poco detectable.
- El individuo es seropositivo.
- En esta etapa, aunque sin síntomas clínicos, se inician alteraciones en el tejido nervioso del corazón y tubo digestivo.
- Aproximadamente la mitad de los pacientes permanece en esta etapa indefinidamente.
- Fase Crónica:
- Se desarrolla en un 20-30% de los afectados, manifestándose 10-20 años después de la infección.
- Caracterizada fundamentalmente por lesiones cardíacas y digestivas.
- Daño Cardíaco (14-45% de los crónicamente infectados): Miocardiopatía.
- Alteraciones del ritmo y conducción (bloqueo de rama derecha, hemibloqueo anterior izquierdo, fibrilación auricular, bloqueo atrio-ventricular completo).
- Aneurisma apical.
- Insuficiencia cardíaca.
- Trombos intramurales, embolias.
- La muerte súbita es frecuente (más del 50%).
- Lesiones del Tubo Digestivo (menos del 10%, 10-21% en países al sur de la región Amazónica):
- Denervación neuronal de los plexos mioentéricos.
- Trastornos de la peristalsis.
- Dilatación del esófago o colon (megaesófago y megacolon).
- Alteraciones del vaciamiento gástrico.
- Trastornos motores de la vesícula biliar y colon.
- Las lesiones del sistema nervioso entérico y central también pueden ocurrir.
Cita Relevante: "La enfermedad de Chagas tiene dos etapas o fases clínicas: una fase aguda y una fase crónica. Muchas personas (del 70 al 80 % de los infectados) son asintomáticas toda su vida, pero de entre un 20 a un 30 % de los afectados esta enfermedad evoluciona a cuadros crónicos sintomáticos asociados a daño lesional en el corazón, tubo digestivo y/o sistemas nerviosos." (OPS/OMS)
5. Diagnóstico:
- El diagnóstico es clínico, epidemiológico y de laboratorio (parasitología y serología).
- Fase Aguda:
- Métodos parasitológicos en sangre:
- Examen directo, tinción de extendidos de sangre, métodos de concentración, cultivo (Método de Strout), xenodiagnóstico.
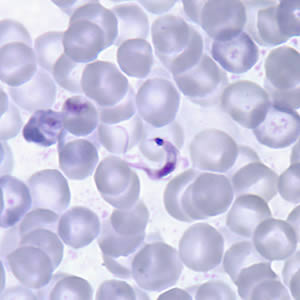
- Alta parasitemia permite la detección directa del parásito (Trypanosoma cruzi).
- Determinación de la seropositivización.
- Fase Crónica:
- Se basa en la evaluación clínica, serología y antecedentes epidemiológicos.
- El diagnóstico definitivo requiere el resultado positivo de al menos dos pruebas serológicas diferentes (ELISA, Inmunofluorescencia Indirecta o Hemaglutinación Indirecta) que detectan anticuerpos específicos.
- PCR: Útil en todas las etapas de la infección (Incani, 2020).
6. Tratamiento:
- Tratamiento etiológico (para eliminar la infección por T.cruzi): Medicamentos: Benznidazol y Nifurtimox.
- Son eficaces para matar el parásito si el tratamiento se inicia durante la fase aguda.
- Todo niño/niña infectados deben ser tratados.
- La eficacia disminuye cuanto más tiempo una persona ha estado infectada, pero todos los pacientes (incluyendo casos crónicos) se benefician de mejores evoluciones clínicas si son tratados etiológicamente.
- No deben administrarse a mujeres embarazadas.
- Ambas drogas tienen efectos colaterales, a veces importantes.
- El tratamiento está indicado en casos con parasitemia o con riesgo importante (agudos, congénitos, trasplantados, transfusión, oral, reactivación, infección accidental) y en niños menores de 12 años, posiblemente extendiéndose a adolescentes y adultos jóvenes si la infección es reciente (últimos 12 años).
- Los casos crónicos menores de 50 años sin cardiomiopatía grave deberían ser tratados.
- La curación se evalúa mediante la negativización de la parasitemia y la reducción o negativización de los títulos de anticuerpos, lo cual puede tardar años o décadas.
- Tratamientos médicos o quirúrgicos no específicos: Para manejar las manifestaciones clínicas crónicas, como trastornos del ritmo cardíaco e insuficiencia cardíaca.
7. Prevención y Control:
- No existe una vacuna para la Enfermedad de Chagas.
- El control integrado de vectores es el método más eficaz de prevenir la enfermedad de Chagas en América Latina.
- Control químico con insecticidas en domicilios infestados.
- Mejora de las casas y su peridomicilio para prevenir la infestación (evitando techos de palma y paredes de bahareque no frisado).
- Medidas preventivas personales (ej. mosquiteros).
- Información, educación y comunicación a la comunidad.
- Tamizaje serológico en donantes de sangre para prevenir la transmisión transfusional.
- Tamizaje serológico en donantes y receptores de órganos y tejidos para prevenir la transmisión por trasplante.
- Tamizaje de Chagas en embarazadas durante controles prenatales para diagnóstico temprano del recién nacido de madres infectadas y estudio de hermanos mayores.
- Buenas prácticas de manufactura e higiene en la preparación, transporte, almacenamiento y consumo de alimentos para prevenir la transmisión oral.
8. Epidemiología y Distribución Geográfica:
- La enfermedad ocurre exclusivamente en el continente americano en su transmisión natural, distribuyéndose en 21 países desde México hasta Argentina donde existan condiciones de vivienda apropiadas para la domiciliación del vector.
- La migración ha llevado la infección a países no endémicos de América y el Mundo.
- Estimados pasados:
- 1990: 100 millones de personas expuestas, 30 millones infectadas, 700.000 nuevos casos anuales, más de 45.000 muertes por año.
- Estimados más recientes (alrededor de 2010-2015):
- 6 a 8 millones de personas infectadas en el mundo (OPS/OMS).
- 7,5 millones de personas infectadas en las Américas (OPS/OMS).
- Alrededor de 1.500.000 personas padecían de cardiopatía chagásica (OPS/OMS).
- Incidencia anual decreció de 700.000 a 28.000 (OPS/OMS).
- Carga de la enfermedad disminuyó significativamente.
- Bolivia ha presentado la tasa de prevalencia serológica nacional más alta (6,75% en 2006 según OPS).
- La enfermedad se ha globalizado con las migraciones, con casos registrados en USA y Europa, predominantemente importados, aunque también se ha documentado transmisión congénita y autóctona limitada.
9. Avances y Desafíos en el Control:
- Desde principios de la década de 1990, los países afectados, junto con la OPS/OMS, han generado un esquema exitoso de cooperación técnica horizontal a través de iniciativas subregionales.
- Estas iniciativas han permitido reducciones importantes en el número de casos agudos y la presencia intradomiciliaria de vectores.
- Logros sustanciales:
- Interrupción de la transmisión vectorial en todo o parte del territorio de 17 países.
- Eliminación de especies alóctonas de vectores.
- Implementación del tamizaje universal de donantes de sangre en los 21 países endémicos.
- Detección y tratamiento de casos congénitos.
- Reducción de la prevalencia en niños y la morbimortalidad.
- Ampliación de la cobertura para el diagnóstico, acceso al tratamiento y atención clínica.
- Ejemplos de eliminación vectorial certificada: Uruguay, Chile, Brasil, Paraguay, Argentina, Guatemala, El Salvador, Honduras, Nicaragua, Costa Rica, Belice, Perú, Colombia, México.
- Desafíos persistentes: Propagación de la enfermedad debido a movimientos migratorios.
- Necesidad de lograr la sostenibilidad de los programas.
- Enfrentamiento de situaciones de emergencia, reemergencia o desastres naturales.
- Necesidad de ampliar la cobertura de diagnóstico y tratamiento adecuados.
- Lograr el acceso universal al tratamiento.
- La Enfermedad de Chagas es una de las 30 afecciones que la Iniciativa de Eliminación de la OPS se ha propuesto eliminar en la Región de las Américas para el año 2030.
Cita Relevante: "Aunque se han logrado avances sustanciales, no todos los países han conseguido alcanzar las metas propuestas y se presentan nuevos desafíos, principalmente la propagación de la enfermedad, debido a movimientos migratorios de personas que viven en países endémicos a países no endémicos, así como también, la necesidad de lograr la sostenibilidad de los programas, el enfrentamiento de situaciones de emergencia y reemergencia o desastres naturales, la necesidad de ampliar la cobertura de diagnóstico y tratamiento adecuados y lograr el acceso universal al tratamiento." (OPS/OMS)
10. Situación en Venezuela (basado principalmente en Incani, 2020):
- La infección fue descrita por primera vez en Venezuela en 1919.
- El programa de control se estableció en 1961, centrado en el control vectorial con insecticidas y el mejoramiento de viviendas rurales.
- La prevalencia nacional cayó significativamente, de 44,5% a 9,2% entre 1958 y 1998.
- Se estima que en el 80% del territorio nacional ha habido posibilidades de transmisión de T. cruzi.
- Estudios más recientes (1992-2002 y 2020) muestran una seroprevalencia global en población rural alrededor del 10-11%.
- Existe transmisión activa, evidenciada por la frecuencia de infección en niños de 0-10 años (8,5% en un estudio, 6,9% en otro).
- La mayor proporción de casos se da en mayores de 50 años, reflejo de la cronicidad de la enfermedad.
- Se han identificado diversos ecosistemas de transmisión, incluyendo zonas llaneras, andinas, piedemontes e incluso zonas semiáridas. Se ha detectado transmisión enzoótica en palmas de cocotero cercanas a viviendas.
- Una nueva situación es la transmisión oral en forma epidémica o microepidémica, registrándose brotes desde 2007, incluso en áreas urbanas.
- Estos brotes suelen ocurrir en zonas donde coexisten reservorios (rabipelados y roedores) y vectores (principalmente P. geniculatus), incluso en urbanizaciones.
- Vehículos de transmisión incriminados han sido jugos de frutas contaminados.
- La clínica en los casos de transmisión oral tiende a ser más sintomática que la vectorial aguda, posiblemente por la mayor carga parasitaria recibida.
- La patología grave más frecuente en brotes orales ha sido la cardíaca (miocarditis, efusión pericárdica, cardiomegalia).
- Desde finales de los años 90, el Programa de Control de la Enfermedad de Chagas en Venezuela se encuentra en estado de desatención, sin realizar actividades seroepidemiológicas ni control de vectores a nivel nacional.
- La Enfermedad de Chagas es de notificación obligatoria en Venezuela.
Cita Relevante: "Desde finales de los años 90s, el Programa de Control de la Enfermedad de Chagas se encuentra en estado de desatención, no realizándose actividades seroepidemiológicas ni control de vectores." (Incani, 2020)
11. Impacto Socioeconómico:
- La enfermedad contribuye a perpetuar el ciclo de pobreza, al reducir la capacidad de aprendizaje, la productividad y la posibilidad de generar ingresos.
Cita Relevante: "Esta enfermedad contribuye a perpetuar el ciclo de pobreza, al reducir la capacidad de aprendizaje, la productividad y la posibilidad de generar ingresos." (OPS/OMS)
12. Respuesta de la OPS/OMS:
- Liderazgo en las iniciativas subregionales de prevención y control.
- Cooperación técnica horizontal entre países.
- Provisión de medicamentos (Nifurtimox y Benznidazol).
- Marco estratégico y plan de acción (resoluciones WHA63.20 y CD50.R17).
- Marco para la eliminación de enfermedades desatendidas (resoluciones CD49.R19 y CD55.R9).
- Iniciativa de Eliminación, con meta de eliminar la Enfermedad de Chagas como problema de salud pública para 2030.
Cita Relevante: "Desde principios de la década de los 90, los países afectados por la enfermedad de Chagas junto con la OPS/OMS, generaron un exitoso esquema de cooperación técnica horizontal entre países, mediante las Iniciativas Subregionales de Prevención y Control de la Enfermedad de Chagas..." (OPS/OMS)
Conclusión:
La Enfermedad de Chagas, si bien ha visto avances significativos en su control en las Américas gracias a los esfuerzos concertados a nivel subregional, sigue siendo un importante problema de salud pública con profundas raíces socioeconómicas. La transmisión vectorial ha disminuido en muchas áreas, pero la persistencia de reservorios, la presencia de vectores en viviendas mal estructuradas y la creciente importancia de la transmisión oral plantean desafíos continuos. La globalización a través de la migración ha extendido la enfermedad a países no endémicos. El acceso limitado al diagnóstico y tratamiento, la necesidad de sostener los programas de control y el impacto de factores sociales y ambientales carenciales son barreras que deben superarse para lograr la meta de eliminación de la Enfermedad de Chagas como problema de salud pública. La situación en Venezuela, marcada por la desatención reciente del programa de control y la emergencia de brotes por transmisión oral, subraya la fragilidad de los avances logrados y la necesidad urgente de reactivar las estrategias de vigilancia y control.
Preguntas sobre Enfermedad de Chagas
¿Qué es la Enfermedad de Chagas y cuál es su agente causal?
La Enfermedad de Chagas, también conocida como tripanosomiasis americana, es una afección parasitaria sistémica y crónica. Es causada por el protozoario flagelado llamado Trypanosoma cruzi, que es un parásito de origen zoonótico. Este parásito tiene la capacidad de infectar diversos tejidos del organismo, con una predilección especial por la musculatura cardíaca, estriada y lisa, el sistema nervioso y el sistema macrofágico histiocitario. Se considera una enfermedad desatendida y está fuertemente vinculada a aspectos socioeconómicos y culturales deficientes.
¿Cómo se transmite la Enfermedad de Chagas?
El principal mecanismo de transmisión de la Enfermedad de Chagas es vectorial. Ocurre a través de hemípteros (chinches) de la subfamilia Triatominae, que son insectos hematófagos. Estos insectos infectan a las personas al depositar sus heces infectadas cerca de la picadura, y el parásito T. cruzi entra al cuerpo cuando la persona instintivamente rasca las heces en la picadura y contamina heridas en la piel o mucosas (como los ojos o la boca). Aunque la transmisión vectorial es la más común, existen otras modalidades importantes:
- Transfusión sanguínea: La transmisión puede ocurrir a través de transfusiones de sangre de donantes infectados.
- Congénita: Las madres infectadas pueden transmitir el parásito a sus hijos durante el embarazo.
- Trasplante de órganos: La infección puede transmitirse a través de trasplantes de órganos o tejidos de donantes infectados.
- Oral: Por la ingestión accidental de alimentos contaminados con T. cruzi, a menudo a través de heces de vectores o la manipulación de carne de animales infectados.
- Accidental en laboratorio: Menos común, pero puede ocurrir en entornos de laboratorio.
¿Cuáles son las fases clínicas de la Enfermedad de Chagas y sus síntomas?
La Enfermedad de Chagas tiene dos etapas o fases clínicas principales:
- Fase Aguda: Esta fase puede ser asintomática o presentar síntomas leves y dura pocas semanas después de la infección. Durante esta etapa, un alto número de parásitos circula en la sangre. Los posibles signos y síntomas incluyen:
- Signos en el sitio de entrada del parásito: un nódulo cutáneo indoloro llamado "chagoma de inoculación" o, en casos de inoculación ocular (raro), el "signo de Romaña" (edema unilateral de los párpados con ganglios linfáticos agrandados cerca de la oreja).
- Fiebre
- Dolor de cabeza
- Náuseas, diarrea o vómitos
- Ganglios linfáticos agrandados
- Dificultad para respirar
- Dolor muscular, abdominal o en el pecho. En personas inmunodeprimidas, la fase aguda puede ser más grave y fatal, manifestándose como meningoencefalitis y pancarditis.
- Fase Crónica: Si la infección no se trata, puede avanzar a la fase crónica, que se inicia después de los síntomas agudos y puede durar años o décadas. Muchas personas permanecen asintomáticas en una fase indeterminada durante toda su vida (70-80%), pero entre un 20% y 30% desarrollan cuadros sintomáticos asociados a daño irreversible en órganos. Los signos y síntomas de la forma crónica pueden incluir:
- Daño cardíaco: Es la complicación más frecuente (alrededor del 30% de los afectados crónicos), manifestándose como miocardiopatía, alteraciones del ritmo y conducción cardíaca, aneurisma apical e insuficiencia cardíaca progresiva.
- Daño digestivo: Menos común (menos del 10% de los pacientes crónicos), pero puede causar dilatación del esófago o colon (megaesófago y megacolon) debido a trastornos motores gastrointestinales, con síntomas como dificultad para tragar y estreñimiento. Las lesiones crónicas del sistema nervioso también pueden presentarse.
¿Cómo se diagnostica la Enfermedad de Chagas?
El diagnóstico de la Enfermedad de Chagas es siempre clínico, epidemiológico y de laboratorio. La metodología de laboratorio depende de la fase de la enfermedad:
- Fase Aguda: Dada la alta concentración de parásitos en la sangre (parasitemia), el diagnóstico se realiza principalmente mediante métodos parasitológicos directos. Esto implica buscar y reconocer el Trypanosoma cruzi en un examen directo de sangre, extendidos de sangre teñidos (método parasitológico directo), o métodos de concentración como el microhematocrito o el método de Strout. También se busca la seropositivización de la serología.
- Fase Crónica: El diagnóstico se basa en la evaluación clínica, los antecedentes epidemiológicos y la serología. El diagnóstico definitivo de la infección por T. cruzi en la etapa crónica requiere un resultado positivo en al menos dos pruebas serológicas diferentes que detecten anticuerpos específicos en el suero del paciente. Las pruebas comunes incluyen ELISA, Inmunofluorescencia Indirecta y Hemaglutinación Indirecta.
La PCR también es una herramienta útil para el diagnóstico en todas las etapas de la infección.
¿Existe una vacuna para la Enfermedad de Chagas y cómo se previene?
No existe una vacuna para prevenir la Enfermedad de Chagas. La prevención se enfoca principalmente en controlar la transmisión a través de diversas estrategias:
- Control integrado de vectores: Este es el método más eficaz en América Latina. Incluye el control químico con insecticidas en viviendas infestadas, la mejora de la infraestructura de las casas y su entorno para prevenir la infestación de triatominos, y medidas preventivas personales como el uso de mosquiteros. La educación y comunicación a la comunidad sobre la enfermedad y su prevención también son cruciales.
- Tamizaje serológico: Es fundamental realizar pruebas serológicas en donantes de sangre para prevenir la transmisión por transfusión. También se realiza tamizaje en donantes de órganos para trasplante.
- Tamizaje en embarazadas: Realizar pruebas de Chagas durante el control prenatal permite identificar a las madres infectadas y trabajar en el diagnóstico temprano y tratamiento de los recién nacidos y hermanos mayores.
- Buenas prácticas de manufactura e higiene alimentaria: Para prevenir la transmisión oral, es importante seguir prácticas de higiene en la preparación, transporte, almacenamiento y consumo de alimentos.
¿Cómo se trata la Enfermedad de Chagas?
La Enfermedad de Chagas puede tratarse etiológicamente con el objetivo de eliminar la infección por T. cruzi utilizando los medicamentos Benznidazol y Nifurtimox.
- Eficacia: Ambos medicamentos son más eficaces para matar el parásito si el tratamiento se inicia durante la fase aguda. Todos los niños infectados deben ser tratados. La eficacia disminuye a medida que la infección se vuelve más crónica, pero se ha demostrado que el tratamiento etiológico en casos crónicos puede mejorar la evolución clínico-patológica.
- Administración y Dosis: Las dosis y la duración del tratamiento varían según la edad y la fase de la enfermedad. Generalmente, el Benznidazol se administra por 30-60 días y el Nifurtimox por 3 meses.
- Contraindicaciones y Efectos Adversos: El Benznidazol y el Nifurtimox no deben administrarse a mujeres embarazadas. Ambos medicamentos pueden tener efectos adversos significativos (hasta en un 40% de los pacientes tratados), que pueden incluir erupciones cutáneas, náuseas, dolor de cabeza, anorexia, neuropatía periférica, mielosupresión y síntomas neurológicos.
- Tratamientos Adicionales: Además del tratamiento antiparasitario, los pacientes con Enfermedad de Chagas, especialmente en la fase crónica sintomática, pueden necesitar tratamientos médicos o quirúrgicos para manejar las complicaciones en órganos como el corazón o el sistema digestivo.
La decisión de tratar a pacientes crónicos, especialmente adultos, implica sopesar los posibles beneficios frente a los riesgos de los efectos adversos, considerando la edad y otras condiciones médicas del paciente.
¿Dónde es endémica la Enfermedad de Chagas y cómo ha evolucionado su distribución?
La Enfermedad de Chagas es endémica en 21 países de las Américas, distribuyéndose desde México hasta Argentina. Su distribución natural está vinculada a la presencia de vectores triatominos y condiciones de vivienda que favorecen su domiciliación, principalmente en zonas rurales y suburbanas.
Aunque es originaria del continente americano, las migraciones de personas infectadas han llevado la enfermedad a países no endémicos tanto en América como en otras partes del mundo (como Estados Unidos y Europa), aunque sin transmisión natural en estos últimos casos.
Desde principios de la década de 1990, ha habido importantes esfuerzos para controlar la enfermedad en la región, lo que ha llevado a reducciones significativas en el número de casos agudos y la presencia de vectores intradomiciliarios en muchas áreas endémicas. Las iniciativas subregionales de prevención y control, con el apoyo de la OPS/OMS, han logrado la interrupción de la transmisión vectorial por especies clave en varios países y la implementación del tamizaje universal en bancos de sangre en los 21 países endémicos. A pesar de estos avances, persisten desafíos como la sostenibilidad de los programas, la respuesta a brotes y reemergencias, y la necesidad de ampliar el acceso al diagnóstico y tratamiento.
¿Cuáles son los factores socioeconómicos y ambientales asociados a la Enfermedad de Chagas?
La Enfermedad de Chagas tiene una firme vinculación con aspectos socioeconómico-culturales deficitarios y se considera una enfermedad desatendida. Varios factores contribuyen a la exposición y transmisión, especialmente en vastas áreas de América Latina:
- Viviendas precarias: Habitar en viviendas mal estructuradas, a menudo con grietas y hendiduras que sirven de refugio para los vectores triatominos, especialmente en zonas rurales y suburbanas. Materiales de construcción como techos de palma y paredes de bahareque no frisado favorecen la infestación.
- Pobreza y falta de recursos: La enfermedad afecta de manera desproporcionada a comunidades con escasos recursos, lo que limita su capacidad para mejorar sus viviendas y acceder a servicios de salud.
- Inestabilidad social y económica: Residir en áreas con inestabilidad social y económica puede exacerbar los factores de riesgo y dificultar la implementación de medidas de control.
- Migración: Los movimientos migratorios de personas infectadas desde áreas endémicas a no endémicas contribuyen a la propagación de la enfermedad a nivel global.
- Trabajo agrícola estacional: Pertenecer a grupos vinculados con el trabajo agrícola estacional puede implicar vivir en condiciones que favorecen el contacto con vectores.
Estos factores crean un ciclo de pobreza, ya que la enfermedad, al reducir la capacidad de aprendizaje y la productividad de las personas afectadas, limita sus posibilidades de generar ingresos y superar las condiciones que los hacen vulnerables.
Autoevaluación
TRIPANOSOMIASIS AMERICANA (Enfermedad de Chagas)
Tripanosomiasis Americana [Playlist]
Bibliografía
Centers for Disease Control and Prevention. (s.f.). DPDx - American Trypanosomiasis. Recuperado el 25 de mayo de 2025, de
Organización Panamericana de la Salud. Temas. https://www.paho.org/es/topics




Comentarios
Publicar un comentario