TOXOPLASMOSIS
Podcast
Videos
Resumen
La toxoplasmosis es una infección parasitaria generalizada causada por Toxoplasma gondii, un protozoo intracelular. Afecta a una amplia variedad de animales de sangre caliente, incluyendo humanos. Si bien la infección es muy común a nivel mundial y a menudo asintomática en individuos inmunocompetentes, puede causar patologías graves en fetos (toxoplasmosis congénita) y personas inmunosuprimidas (particularmente encefalitis toxoplásmica). El ciclo de vida del parásito involucra a los felinos como hospedadores definitivos que eliminan ooquistes en sus heces, y a otros animales (incluidos humanos) como hospedadores intermediarios que adquieren la infección al ingerir ooquistes o quistes tisulares en carne poco cocida. El diagnóstico se basa principalmente en serología, aunque la detección de ADN por PCR es crucial en casos congénitos y en inmunosuprimidos. El tratamiento se reserva para casos activos y sintomáticos, y no existen medicamentos que eliminen los quistes tisulares de la infección crónica. La prevención se centra en evitar la exposición a ooquistes en heces de gato y a quistes tisulares en carne cruda o poco cocida. La prevalencia varía geográficamente, con tasas altas en muchas partes del mundo.
- Agente Causal y Definición:
- La toxoplasmosis es causada por Toxoplasma gondii, un protozoo parásito intracelular.
- Pertenece al filo Apicomplexa, un grupo que incluye a otros parásitos importantes como Plasmodium y Cryptosporidium.
- La infección es generalizada, afectando múltiples órganos y tejidos con células nucleadas.
- Es muy frecuente tanto en humanos como en una amplia variedad de animales de sangre caliente.
- "Toxoplasma gondii is a protozoan parasite that infects most species of warm-blooded animals, including humans, and causes the disease toxoplasmosis." (CDC)
- "La toxoplasmosis es una infección generalizada que afecta múltiples órganos y tejidos con células nucleadas, en el hombre y una gran variedad de animales de sangre caliente, causada por el parásito intracelular Toxoplasma gondii." (Incani)
- Ciclo de Vida y Transmisión:
- T. gondii tiene un ciclo de vida complejo con etapas asexuales y sexuales.
- Los felinos (gatos domésticos y silvestres) son los únicos hospedadores definitivos conocidos.
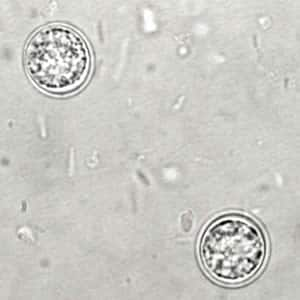
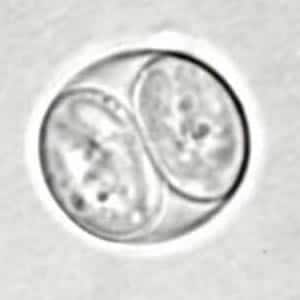
- Los gatos eliminan ooquistes no esporulados en sus heces durante 1 a 3 semanas. Estos ooquistes se vuelven infectivos después de esporular en el medio ambiente (1-5 días).
- Los hospedadores intermediarios (incluyendo aves, roedores y otros animales) se infectan al ingerir ooquistes del suelo, agua o vegetación contaminada.
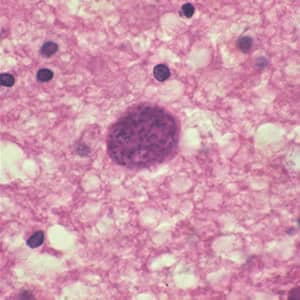
- En los hospedadores intermediarios, los ooquistes se transforman en taquizoítos que se diseminan y luego forman quistes tisulares (bradizoítos), comúnmente en músculo, corazón, cerebro y ojos. Estos quistes pueden persistir de por vida.
- Los gatos se infectan al consumir hospedadores intermediarios que contienen quistes tisulares o al ingerir ooquistes esporulados.
- Los humanos pueden infectarse por varias vías:
- Ingesta de carne cruda o poco cocida que contiene quistes tisulares.
- Consumo de alimentos o agua contaminados con heces de gato (ooquistes) o por contacto con muestras ambientales contaminadas (como tierra o al cambiar la caja de arena de un gato).
- Transfusión sanguínea o trasplante de órganos.
- Transplacentaria de madre a feto durante un primoinfección aguda en el embarazo.
- "Humans can become infected by any of several routes: Eating undercooked meat of animals harboring tissue cysts. Consuming food or water contaminated with cat feces or by contaminated environmental samples... Blood transfusion or organ transplantation. Transplacentally from mother to fetus." (CDC)
- "Se transmite a través de la ingesta de ooquistes en el suelo, provenientes de las heces de felinos, y en consecuencia contaminantes de vegetales y agua, o también de carne de animales infectados..." (Incani)
- "Hay indicios que hablan a favor de la ingesta de ooquistes como el mecanismo principal de infección." (Incani)
- "Es casi imposible evitar entrar en contacto natural con este parásito en algún momento en la vida." (Incani)
- Morfología:
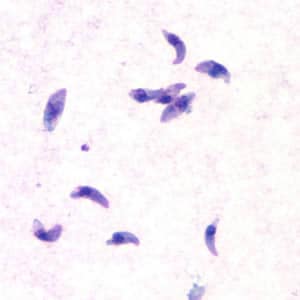
- "Los taquizoítos (trofozoítos) de Toxoplasma gondii miden aproximadamente 4-8 μm de largo por 2-3 μm de ancho, con un extremo anterior cónico, un extremo posterior romo y un núcleo grande. Se pueden encontrar en varios sitios en todo el cuerpo del hospedador." (CDC)
- Patología y Presentación Clínica:
- La mayoría de las infecciones en personas inmunocompetentes son asintomáticas.
- En un 10-20% de los casos agudos en inmunocompetentes, pueden presentarse linfadenopatía cervical o síntomas similares a la gripe, generalmente autolimitados.
- Los órganos mayormente afectados en la infección son el tejido linfático, cerebro, ojo, corazón, hígado y pulmón.
- "Acquired infection with Toxoplasma in immunocompetent persons is generally an asymptomatic infection. However, 10% to 20% of patients with acute infection may develop cervical lymphadenopathy and/or a flu-like illness." (CDC)
- "La forma asintomática es la más frecuente, pasando la infección totalmente desapercibida posiblemente en más del 90% de los casos." (Incani)
- En pacientes inmunosuprimidos, la toxoplasmosis puede ser grave y potencialmente mortal, a menudo debido a la reactivación de una infección crónica latente.
- La encefalitis toxoplásmica es la causa más común de lesiones intracerebrales en pacientes con SIDA con recuentos bajos de linfocitos CD4. También pueden presentar retinocoroiditis, neumonitis u otras enfermedades sistémicas.
- "Immunodeficient patients often have central nervous system (CNS) disease but may have retinochoroiditis, pneumonitis, or other systemic disease. In patients with AIDS, toxoplasmic encephalitis is the most common cause of intracerebral mass lesions and is thought to usually be caused by reactivation of chronic infection." (CDC)
- "La infección generalizada trae problemas graves al inmunodeprimido..." (Incani)
- La toxoplasmosis congénita resulta de una infección aguda primaria de la madre durante el embarazo y puede causar lesiones fetales significativas, incluyendo aborto, partos prematuros, muerte intrauterina, retardo del crecimiento, neumonía, hepatoesplenomegalia, trombocitopenia y daño oftálmico y neurológico (meningoencefalitis, hidro/microcefalia, calcificaciones, retardo psicomotor, epilepsia).
- La gravedad y la incidencia de la toxoplasmosis congénita varían con el trimestre del embarazo en que se adquiere la infección (el riesgo de transmisión aumenta en los últimos trimestres, pero la gravedad tiende a ser mayor si la infección ocurre en el primer trimestre).
- Muchos bebés con infección congénita sub clínica al nacer desarrollarán síntomas y signos más tarde.
- "Congenital toxoplasmosis results from an acute primary infection acquired by the mother during pregnancy. The incidence and severity of congenital toxoplasmosis vary with the trimester during which infection was acquired." (CDC)
- "Es causante de importantes lesiones fetales." (Incani)
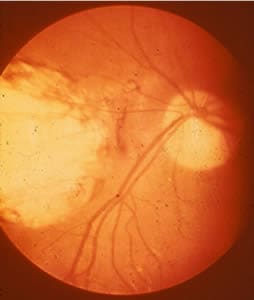
- La toxoplasmosis ocular puede ser congénita o adquirida y es una causa importante de retinocoroiditis. Las lesiones congénitas suelen ser bilaterales, mientras que las adquiridas son unilaterales y focales. La cicatrización de las lesiones retinianas es una placa hiperpigmentada.
- "Ocular Toxoplasma infection, an important cause of retinochoroiditis in the United States, can be the result of congenital infection, or infection after birth." (CDC)
- "La toxoplasmosis ocular. Puede ser congénita o adquirida... En la congénita, las lesiones son habitualmente bilaterales... La toxoplasmosis ocular adquirida es unilateral, focal..." (Incani)
- Genotipos:
- Se han descrito y se siguen describiendo genotipos de T. gondii asociados a regiones geográficas y a la capacidad de generar mayor o menor patología (virulencia).
- En Suramérica y la Amazonia existe una amplia variación de tipos, más allá de los tres genotipos básicos (Tipo I, II, III).
- El genotipo I es considerado experimentalmente el más virulento en ratones, mientras que el II y III son menos virulentos y más frecuentes en USA y Europa.
- En Guayana Francesa, genotipos particulares han causado daño significativo y muerte en adultos aparentemente inmunocompetentes.
- En USA, el serotipo II y NE-II se asocian a toxoplasmosis congénita, siendo NE-II asociado a prematuridad y severidad al nacer.
- En Suramérica y África, la mayor variedad de genotipos podría contribuir a la alta prevalencia de seropositividad y enfermedad ocular.
- "Se han descrito, y continúan describiéndose, genotipos de este parásito asociados a regiones geográficas y a capacidades de generar mayor o menor patología." (Incani)
- Diagnóstico:
- El diagnóstico clínico es difícil debido a la heterogeneidad de síntomas.
- El método de diagnóstico más rutinario y frecuente es la serología, que detecta anticuerpos específicos (IgG e IgM).
- Una IgG positiva indica infección en algún momento. Una IgM positiva sugiere infección reciente, pero puede persistir hasta 18 meses y la interpretación puede ser difícil.
- En situaciones críticas como el embarazo, se recomiendan pruebas de seguimiento o confirmatorias (panel de pruebas serológicas).
- Para infecciones congénitas in utero y encefalitis toxoplásmica en pacientes con VIH, la detección de ADN por PCR es una herramienta importante.
- La observación directa de parásitos en muestras (biopsias, lavado broncoalveolar) es posible pero menos común.
- En neonatos, se buscan anticuerpos IgG, IgM e IgA. Los IgM e IgA reflejan la respuesta inmune del bebé, ya que no cruzan la placenta, pero pueden darse falsos negativos si la infección fue muy temprana. Se recomienda enviar muestras a laboratorios especializados.
- En pacientes con VIH y toxoplasmosis cerebral activa, la IgG suele ser positiva; su ausencia hace el diagnóstico menos probable. Las IgM suelen ser negativas. Los títulos cuantitativos de anticuerpos no son útiles para el diagnóstico en estos casos.
- "Diagnosis is usually achieved by serology, although tissue cysts may be observed in stained biopsy specimens." (CDC)
- "Diagnosis of congenital infections can be achieved by detecting T. gondii DNA in amniotic fluid using molecular methods such as PCR." (CDC)
- "The detection of Toxoplasma-specific antibodies is the primary diagnostic method..." (CDC)
- "Lo más frecuente es el uso de técnicas serológicas, dentro de lo posible, que midan IgM (infección activa) e IgG (infección pasada)." (Incani)
- "La visualización del parásito en las lesiones es muy difícil, por lo que se está utilizando modernamente la PCR en los sitios donde sea viable realizarla, en particular la PCR en líquido amniótico en embarazadas." (Incani)
- Tratamiento:
- El tratamiento se indica en casos de enfermedad activa (visceral, encefálica, ocular), madres embarazadas con primoinfección, niños con infección congénita e inmunosuprimidos con activación.
- Las primoinfecciones febriles con adenopatías sin otras manifestaciones generalmente no se tratan.
- No existen drogas activas contra los quistes tisulares de la infección crónica.
- Los esquemas de tratamiento suelen basarse en combinaciones de pirimetamina y sulfa. Otros regímenes incluyen trimetoprim/sulfa, dapsona/pirimetamina, clindamicina/pirimetamina.
- La espiramicina es el único tratamiento disponible para mujeres embarazadas para reducir la transmisión al feto, aunque después de la semana 16 y si se confirma infección fetal, se cambia al esquema de pirimetamina, sulfa y ácido folínico.
- Se puede añadir ácido folínico a la combinación de pirimetamina/sulfa para contrarrestar la depresión de la médula ósea.
- Los esteroides (como prednisona) deben añadirse en casos de coriorretinitis.
- "The clinical course is usually benign and self-limited; symptoms usually resolve within a few weeks to months." (CDC)
- "El tratamiento de la toxoplasmosis debe indicarse cuando hay enfermedad activa visceral, encefálica, ocular, madre embarazada con primoinfección, niño con infección congénita, o inmunosuprimidos con activación de la infección." (Incani)
- "No existen drogas activas contra los quistes tisulares de la infección crónica." (Incani)
- "Pirimetamina/sulfa combinadas es la primera y más eficiente opción..." (Incani)
- "Spiramicina, único tratamiento disponible en pacientes embarazadas..." (Incani)
- Distribución Geográfica y Prevalencia:
- La distribución de la toxoplasmosis es mundial, en áreas tropicales y templadas, desarrolladas y subdesarrolladas.
- Se estima que infecta a aproximadamente un tercio de la población mundial.
- "Serologic prevalence data indicate that toxoplasmosis is one of the most common human infections throughout the world." (CDC)
- La prevalencia varía significativamente por región y está influenciada por hábitos alimenticios (consumo de carne cruda o poco cocida) y la exposición a heces de gato y tierra contaminada.
- Prevalencia en USA: 12.4% en personas >6 años (NHANES 2009–2010), 9.1% en mujeres de 15–44 años. Encuestas anteriores mostraban tasas más altas (22.5% en NHANES III).
- Prevalencia en Francia: alta, relacionada con el consumo de carne cruda.
- Prevalencia en Centroamérica: alta, relacionada con la frecuencia de gatos callejeros y clima favorable para los ooquistes.
- Prevalencia en Europa continental, Centro y Suramérica: 30-60%.
- Prevalencia en embarazadas en Brasil: 50-80%.
- En Venezuela, estudios serológicos han mostrado tasas de prevalencia que varían entre 33% y 63% en diferentes comunidades, con una tasa de positividad a IgM (infección activa) que varía entre 0.7% y 22%.
- La toxoplasmosis es una causa importante de enfermedades transmitidas por alimentos en USA, siendo la segunda causa de hospitalizaciones y la tercera de muertes reportadas para 2011.
- Se estimó una incidencia anual global de toxoplasmosis congénita de 190.100 casos en 2013, con una carga de enfermedad significativa (DALYS). La mayor carga se observa en Suramérica, Medio Oriente y África.
- Se estima que más de 13 millones de personas infectadas con VIH y seropositivas a Toxoplasma están en riesgo de toxoplasmosis cerebral, principalmente en África Subsahariana.
- La toxoplasmosis no es de notificación obligatoria en Venezuela y no existe un programa de control específico.
- Prevención y Control:
- Las medidas de prevención son limitadas debido a la amplia distribución.
- Evitar la ingesta de ooquistes: Lavarse las manos frecuentemente (especialmente después de contacto con tierra o cajas de arena), lavar adecuadamente las verduras crudas.
- Controlar la infección en gatos: Evitar alimentar a los gatos con carne cruda, mantener a los gatos callejeros alejados de los recintos humanos. El desarrollo de una vacuna para gatos que impida la producción de ooquistes sería una meta ideal.
- Evitar la ingesta de quistes tisulares: Cocinar adecuadamente la carne (destruye los quistes a 60°C). La congelación y descongelación también podrían destruirlos. Es difícil controlar hábitos culturales de consumo de carne cruda.
- Mujeres embarazadas seronegativas deben ser particularmente cuidadosas: usar guantes al manipular tierra o heces de gato y al preparar carne, lavarse las manos con frecuencia.
- En inmunosuprimidos seropositivos, se debe considerar el tratamiento profiláctico.
- Existe debate sobre si niñas mayores seronegativas deberían aplicar medidas estrictas de control, dado el riesgo de llegar al embarazo sin inmunidad en ausencia de una vacuna.
- "Para el caso de la transmisión por ooquistes a través del suelo, el lavado de las manos frecuente y antes de comer... Así mismo, el adecuado lavado de los vegetales que se ingieren crudos, es deseable." (Incani)
- "El control de la infección en los gatos sería la meta ideal para la prevención de esta infección... es deseable evitar alimentar los gatos con productos cárnicos crudos y mantener los gatos realengos fuera de los recintos humanos." (Incani)
- "Para el caso de la transmisión por ingesta de carne... es la adecuada cocción el mecanismo ideal, ya que los quistes son destruidos a 60°C." (Incani)
Puntos Adicionales Importantes:
- La toxoplasmosis crónica silente se ha asociado con trastornos cognitivos y neuropsiquiátricos.
- La prevalencia y gravedad de la toxoplasmosis cerebral en pacientes con SIDA ha disminuido significativamente con el advenimiento de las terapias antirretrovirales altamente efectivas.
- La información sobre la transmisión vertical y la patología en niños nacidos de madres VIH+ y coinfectadas con toxoplasmosis crónica es compleja y a veces conflictiva, influenciada por el estado del VIH, el recuento de CD4 de la madre, el momento de la infección por Toxoplasma, la medicación profiláctica y la cepa de Toxoplasma.
Conclusión:
La toxoplasmosis es una parasitosis de gran impacto global debido a su alta prevalencia y las graves consecuencias que puede tener en poblaciones vulnerables como fetos y personas inmunosuprimidas. Aunque la infección es a menudo asintomática, su capacidad de reactivación y los daños causados por la infección congénita y la afectación de órganos vitales resaltan la importancia de la comprensión de su epidemiología, diagnóstico y prevención. El complejo ciclo de vida que involucra a los felinos y múltiples vías de transmisión en humanos dificultan su control efectivo a nivel poblacional, haciendo que las medidas preventivas individuales y el tratamiento de casos activos sean los pilares del manejo actual. El estudio de los genotipos del parásito y su relación con la patogenicidad son áreas de investigación importantes, especialmente en regiones con alta diversidad genética de T. gondii.
Preguntas sobre toxoplasmosis:
¿Qué es la toxoplasmosis y cuál es su agente causal?
La toxoplasmosis es una infección generalizada que afecta a una amplia variedad de animales de sangre caliente, incluyendo a los humanos. Es causada por un parásito intracelular llamado Toxoplasma gondii, que pertenece al filo Apicomplexa, un grupo de protozoarios parásitos. Este parásito puede afectar múltiples órganos y tejidos con células nucleadas, siendo los más afectados el tejido linfático, cerebro, ojo, corazón, hígado y pulmón.
¿Cómo se transmite Toxoplasma gondii a los humanos?
La transmisión a los humanos puede ocurrir de varias maneras. La principal ruta de infección es la ingesta de ooquistes maduros (formas infecciosas del parásito) que se encuentran en el suelo, agua o vegetales contaminados con heces de felinos. Los felinos, especialmente los gatos domésticos, son los únicos huéspedes definitivos conocidos donde el parásito se reproduce sexualmente y elimina ooquistes en sus heces. Otra vía importante de transmisión es el consumo de carne poco cocida o cruda que contiene quistes tisulares con bradizoítos del parásito, provenientes de animales infectados para consumo humano o caza silvestre. Además, la transmisión puede ocurrir a través de transfusiones de sangre o trasplantes de órganos, y transplacentariamente de una madre infectada a su feto (toxoplasmosis congénita).
¿Cuál es el papel de los gatos en el ciclo de vida de Toxoplasma gondii?
Los gatos domésticos y sus parientes son los únicos huéspedes definitivos conocidos para Toxoplasma gondii. En el intestino de los felinos, el parásito completa su ciclo de vida sexual, lo que resulta en la eliminación de ooquistes no esporulados en las heces. Estos ooquistes se vuelven infecciosos después de 1 a 5 días en el medio ambiente. Los gatos se infectan al ingerir huéspedes intermediarios (como roedores o aves) que contienen quistes tisulares, o al ingerir ooquistes esporulados directamente del ambiente. Aunque la eliminación de ooquistes suele durar solo de 1 a 3 semanas, se pueden liberar grandes cantidades.
¿Cuáles son los síntomas de la toxoplasmosis en personas inmunocompetentes?
En personas con un sistema inmunitario sano, la infección por Toxoplasma gondii es generalmente asintomática en la mayoría de los casos (posiblemente más del 90%). Sin embargo, un porcentaje menor (10% a 20%) puede desarrollar síntomas que se asemejan a una enfermedad viral aguda, como linfadenopatía (inflamación de los ganglios linfáticos), que es la forma sintomática más frecuente, y/o síntomas similares a la gripe. El curso clínico suele ser benigno y autolimitado, con síntomas que se resuelven en semanas o meses. En casos raros, puede ocurrir infección ocular con pérdida de la visión.
¿Cómo afecta la toxoplasmosis a personas inmunodeficientes y a fetos?
En personas con sistemas inmunitarios comprometidos (como pacientes con VIH/SIDA o aquellos bajo tratamiento inmunosupresor), la toxoplasmosis puede ser grave y a menudo es causada por la reactivación de una infección crónica. Las manifestaciones clínicas pueden incluir enfermedad del sistema nervioso central (SNC), retinocoroiditis, neumonitis y otras enfermedades sistémicas. La encefalitis toxoplásmica es una causa común de lesiones cerebrales en pacientes con SIDA. La toxoplasmosis congénita ocurre cuando una madre adquiere una infección primaria durante el embarazo y la transmite al feto. La incidencia y gravedad varían según el trimestre de la infección. La infección congénita puede resultar en abortos, partos prematuros, muerte intrauterina, y embriopatías o fetopatías de diversa gravedad, con posibles secuelas neurológicas y oculares (como coriorretinitis) que pueden ser incapacitantes.
¿Cómo se diagnostica la toxoplasmosis?
El diagnóstico de la toxoplasmosis se realiza principalmente mediante pruebas serológicas, que detectan anticuerpos específicos contra Toxoplasma. La detección de anticuerpos IgG indica una infección en algún momento, mientras que la detección de anticuerpos IgM puede sugerir una infección reciente, aunque pueden persistir durante muchos meses. En situaciones críticas, como en mujeres embarazadas, se recomiendan pruebas de seguimiento o confirmatorias, que analizan un panel de anticuerpos para determinar el momento probable de la infección. También se puede diagnosticar mediante la observación directa de parásitos en muestras de tejido o fluidos corporales, o mediante la detección de material genético del parásito utilizando técnicas moleculares como la PCR, que es útil para diagnosticar infecciones congénitas en líquido amniótico o encefalitis en pacientes con VIH. En la toxoplasmosis ocular, la visualización de las lesiones mediante examen oftalmológico es muy orientadora.
¿Cómo se trata la toxoplasmosis?
El tratamiento de la toxoplasmosis se indica en casos de enfermedad activa visceral, encefálica, ocular, en madres embarazadas con primoinfección, niños con infección congénita, o en personas inmunosuprimidas con reactivación de la infección. Las infecciones asintomáticas o con síntomas leves sin otras manifestaciones generalmente no requieren tratamiento. Los medicamentos utilizados incluyen combinaciones como pirimetamina y sulfa (con suplemento de ácido folínico para contrarrestar efectos secundarios), trimetoprim/sulfa, dapsona/pirimetamina, clindamicina/pirimetamina y espiramicina (especialmente en embarazadas). En casos de coriorretinitis, se pueden añadir esteroides como la prednisona. No existen tratamientos efectivos contra los quistes tisulares de la infección crónica.
¿Cómo se puede prevenir la infección por Toxoplasma gondii?
Las medidas de prevención, dada la amplia distribución del parásito, pueden ser limitadas pero importantes. Se recomienda lavar bien las manos frecuentemente, especialmente después de manipular tierra o trabajar en el jardín, y antes de comer, particularmente si hay gatos en la casa o el vecindario. Es fundamental lavar adecuadamente los vegetales que se consumen crudos. Evitar alimentar a los gatos con carne cruda y controlar la presencia de gatos callejeros puede ayudar a reducir la eliminación de ooquistes. Para prevenir la transmisión por ingesta de carne, la cocción adecuada de la carne es el método ideal, ya que los quistes se destruyen a 60°C; la congelación y descongelación también pueden ayudar. Las mujeres embarazadas seronegativas deben ser especialmente cuidadosas al manipular tierra o cajas de arena de gatos, y al preparar carnes, utilizando guantes y lavándose las manos. Para las personas inmunosuprimidas seropositivas, se puede considerar el tratamiento profiláctico para prevenir la reactivación de la infección.
Autoevaluación
Bibliografía
Centers for Disease Control and Prevention. (s.f.). DPDx - Toxoplasmosis. Recuperado el 25 de mayo de 2025, de
Organización Panamericana de la Salud. Temas. https://www.paho.org/es/topics


Comentarios
Publicar un comentario